朋友圈炸了!一则来自大洋彼岸的抗癌药获批信息引爆朋友圈。
“广谱”、“抗癌”、“治愈率高达75%”……
这些关键词完美吸引了具有“癌症恐惧症”的中国网民的眼球……

39健康网第一时间编译了FDA的相关信息,并联系了该药的所属药企拜耳公司,却意外发现:
75%是缓解率,而不是治愈率!
所谓的“广谱”针对的是特定的基因突变癌症人群,而不是所有癌症患者!
同时,这款新药的目标对象是肿瘤细胞中发生两个基因特定融合的患者,而与其所患肿瘤的类型无关。这种基因融合会发生在各种各样的癌症中,但十分罕见,仅占不到1%的癌症!
@美国MD安德森癌症中心张玉蛟教授,也在微博上向网友解释:
75%有效率绝不是治愈率,而是指患者的病情稳定或者缩小或者消失。

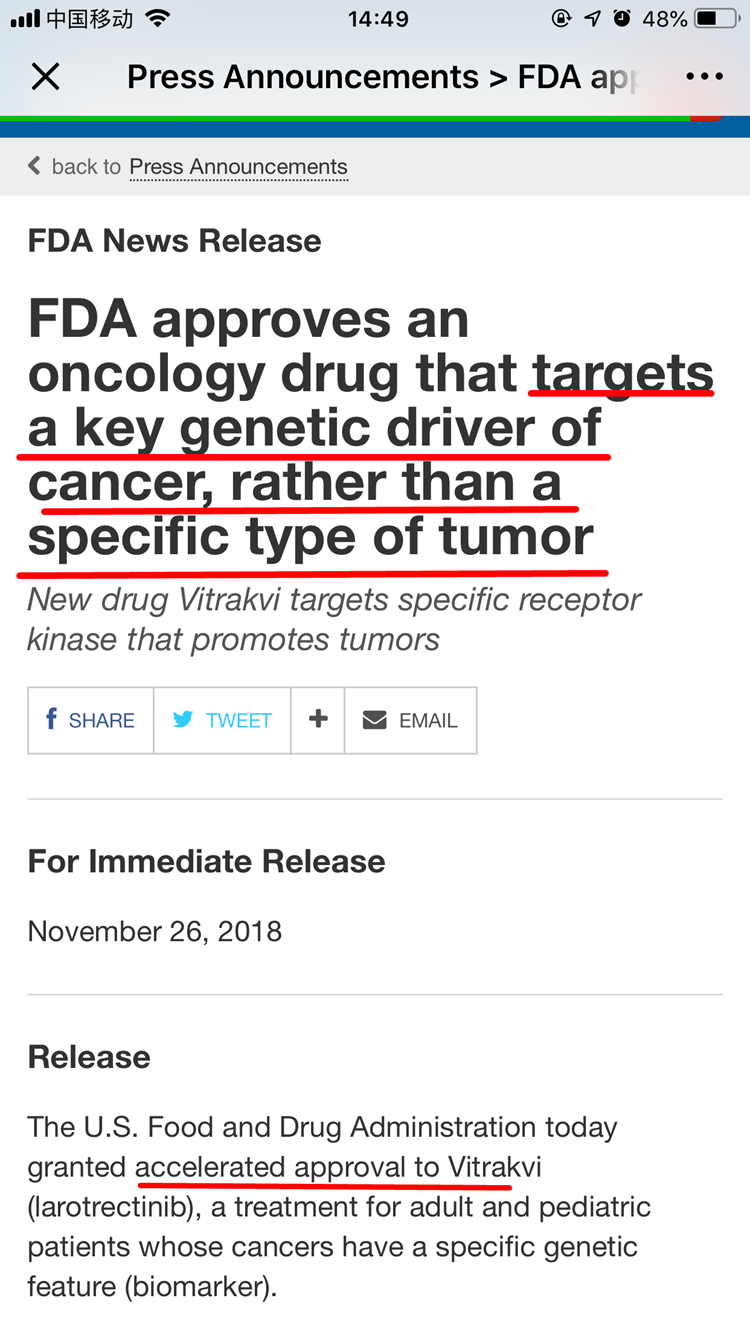
39健康网浏览美国食品药品监督管理局(Food and Drug Administration)官网发现,美国时间11月26日,FDA确实批准了一款名为Vitrakvi(larotrectinib)的抗癌新药,而且是“加速批准”。这是一款针对癌症的关键遗传因素,而非特定类型肿瘤的肿瘤药物。由拜耳和Loxo Oncology共同研发。
官网发文中还提到,这是一款用于治疗患有实体肿瘤的成人和儿童患者的药物(这种实体肿瘤携带了NTRK基因融合,且没有产生已知的获得性抗性突变,后期会发生转移,手术切除会引发高发病率,目前没有有效替代方案和治疗进展)。
也就是说,这种药物的有效人群非常明确——肿瘤中存在NTRK基因融合的患者。
同时,拜耳公司的官方消息也指出,Larotrectinib是首个用于治疗NTRK基因融合晚期实体瘤患者的口服TRK抑制剂。具体说来,对于无已知耐药突变的,广泛转移或局部手术治疗效果不好的,现有治疗方案进展或无可替代治疗方案的NTRK基因融合成人和儿童实体瘤患者可使用此药。
据了解,NTRK基因融合属于染色体改变,其结果会产生构象激活的异常TRK融合蛋白,其作用为肿瘤驱动因子,在肿瘤细胞系中可促进肿瘤细胞的增殖和存活。而Larotrectinib正是可专门抑制这些蛋白的具有中枢神经系统活性的TRK抑制剂。
“NTRK基因融合是一种罕见的癌症驱动因子,FDA批准Larotrectinib对于此类肿瘤的治疗是一个重要的里程碑。我曾经亲自见证Larotrectinib的治疗,它是专门为这种致癌驱动基因而量身定制的,而与患者的年龄和肿瘤类型无关。” Sloan Kettering 癌症中心早期药物开发服务主任,暨Larotrectinib一项临床试验的全球研究负责人David Hyman博士介绍,“现在,我们有了首个已获批的针对这种基因改变的且与肿瘤类型无关治疗药物。”
此外,FDA发文还提到了关于该药的疗效问题,在对55名患有实体肿瘤的儿童和成人患者的三项临床试验中,Larotrectinib在不同类型的实体肿瘤中总缓解率为75%。且药效较为持久,其中73%用药患者药效持续了至少6个月,39%的用药患者药效持续了一年以上。

而在上述临床试验中,接受Larotrectinib的患者也出现了常见的副作用,包括疲劳,恶心,咳嗽,便秘,腹泻,头晕,呕吐以及肝脏中AST和ALT酶血液水平升高。该文建议卫生保健提供者在治疗的第一个月内要每两周监测一次患者的ALT和AST肝脏水平,然后按月和临床指示进行监测。同时指出,孕妇或哺乳期妇女不应服用Larotrectinib,因为它可能对正在发育的胎儿或新生儿造成伤害。
拜耳公司则表示在支持此次获批的临床试验中,Larotrectinib在多种独特的肿瘤类型中显示了临床获益,包括肺癌、甲状腺癌、黑色素瘤、GIST、结肠癌、软组织肉瘤、涎腺肿瘤和婴儿纤维肉瘤。可以发现,这些肿瘤类型大多是发病率较低的瘤种。
关于TRK融合肿瘤的诊断,拜耳公司表示可通过特定的检测方法,包括使用新一代测序技术(NGS)和荧光原位杂交(FISH)对NTRK基因融合进行鉴定。
科罗拉多大学癌症中心胸部肿瘤研究计划主任Doebele是发现TRK基因融合对癌症具有驱动作用的医生之一,他曾参与了上述三项临床试验,对于Larotrectinib的诞生,他表示这意味着抗癌药物的研发有了一个新的方向。“我们发现并证实了新的癌症驱动基因的存在,并发明了一种检测方法,还找出了存在TRK融合的癌症,然后进行药物设计和临床前实验。”
而FDA此次对Larotrectinib进行了优先审评。据悉,优先审评适用于那些可以显著提高治疗严重疾病的有效性或安全性的药物。此前FDA也先后给予该药物突破疗法、罕见儿科疾病药品和孤儿药的资格认定。
美国FDA局长Scott Gottlieb表示:“Larotrectinib的批准上市,是治疗癌症的疗法从基于人体起源组织向基于肿瘤遗传特征转变的重要一步。”

值得注意的是,关于该药物获批的消息最初来源于几个不知名的微信公众号,且内容不够准确,39健康网一早看到消息后即向拜耳公司求证,直到下午官方公告姗姗来迟。虽然该药物批准上市的消息让很多人振奋不已,也的确是抗癌药物的一次重要发现,特别是作为一种跨瘤种的治疗药物出现。但作为普通人的我们,最重要的是首先搞清楚Larotrectinib的真正适用人群:针对的是特定的基因突变癌症人群,而不是所有癌症患者!而且这种药物的有效人群非常明确——肿瘤中存在NTRK基因融合的患者。
当然,不可否认的是,不管适用人群有多少,该药的获批都是人类与癌症斗争的又一次胜利。但纵观整个癌症抗争史,这也只能算是一个特定领域的小小胜利。所以,让朋友圈狂欢的75%治愈率只能算是一个不那么美丽的误会,而距离最终战胜癌症的终极目标,截止目前来看,还任重道远。
39健康网(www.39.net)专稿,未经书面授权请勿转载。

 39健康网
39健康网 癌症血小板升高吗能治好吗
癌症血小板升高吗能治好吗 癌症能治好吗澄清癌症的7大误区
癌症能治好吗澄清癌症的7大误区 癌症是不是一定有肿瘤?
癌症是不是一定有肿瘤? 癌症呕吐是什么样的症状
癌症呕吐是什么样的症状 癌症患者出现抽搐还能活多久
癌症患者出现抽搐还能活多久 得了癌症,不能吃鸽子肉?提醒:3种“发物”真的要少吃
得了癌症,不能吃鸽子肉?提醒:3种“发物”真的要少吃 睡觉时枕头多高、床多硬最好?
睡觉时枕头多高、床多硬最好? 左眼皮老跳到底是怎么回事?
左眼皮老跳到底是怎么回事? 辟谣 | 医生做手术不穿内裤?患者要全裸?别害羞,真相其实很简单
辟谣 | 医生做手术不穿内裤?患者要全裸?别害羞,真相其实很简单




















